Bộ Y tế công bố giá bán của 3 loại thuốc điều trị COVID-19 do VN sản xuất
- Minh Sơn
- •
Năm ngày sau khi cấp phép lưu hành, giá bán 3 loại thuốc chứa hoạt chất Molnupiravir điều trị bệnh viêm phổi Vũ Hán (COVID-19) sản xuất trong nước được Cục Quản lý Dược (Bộ Y tế Việt Nam) công bố. Mức giá từ xấp xỉ 9.000 đồng đến 12.500 đồng/viên. 
Theo công bố của Cục Quản lý Dược (Bộ Y tế) vào chiều 23/2, giá bán 3 loại thuốc chứa hoạt chất Molnupiravir điều trị COVID-19 lần lượt như sau:
Thuốc Molravir 400 (400 mg) dạng viên nang cứng do Công ty CP Dược phẩm Boston Việt Nam sản xuất: Giá bán 11.500 đồng/viên. Dạng hộp có loại 1, 2 và 5 vỉ (10 viên/vỉ).
Thuốc Movinavir (200 mg) dạng viên nang của Công ty CP hóa dược phẩm Mekophar: Giá bán 8.675 đồng/viên. Dạng hộp 10 vỉ x 10 viên.
Thuốc Molnuporavir Stella 400 (400 mg) dang viên nang cứng của Công ty TNHH liên doanh Stellapharm- chi nhánh 1: Giá bán 12.500 đồng/viên, mỗi hộp 1 vỉ hoặc 2 vỉ x 10 viên.
Ngày 17/2, Cục trưởng Cục Quản lý Dược Vũ Tuấn Cường đã cấp giấy đăng ký lưu hành 3 loại thuốc chứa Molnupiravir được sản xuất tại Việt Nam cho điều trị bệnh Covid-19, gồm:
– Molravir 400: hàm lượng Molnupiravir 400 mg, dạng viên nang cứng, tuổi thọ 6 tháng, do Công ty CP dược phẩm Boston Việt Nam sản xuất;
– Movinavir: hàm lượng 200 mg Molnupiravir, dạng viên nang cứng, tuổi thọ 6 tháng, do Công ty CP hóa dược phẩm Mekophar sản xuất;
– Molnuporavir Stella 400: hàm lượng 400 mg Molnupiravir, dạng viên nang cứng, tuổi thọ 8 tháng do Công ty TNHH Liên doanh Stellapharm- chi nhánh 1 sản xuất.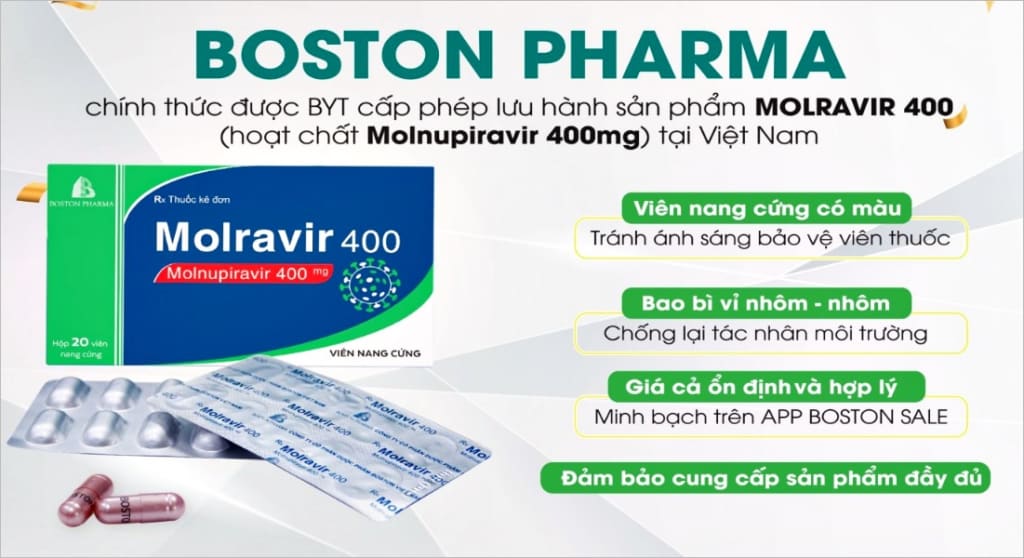
Việc cấp phép cho các loại thuốc này có hiệu lực 3 năm từ ngày ký ban hành Quyết định. Đối với các trường hợp xảy ra phản ứng có hại của thuốc (nếu có), Cục này đề nghị gửi báo cáo về Trung tâm Quốc gia về thông tin thuốc và theo dõi phản ứng có hại của thuốc (ở Hà Nội) hoặc Trung tâm khu vực về thông tin thuốc và theo dõi phản ứng có hại của thuốc (ở TPHCM).
Báo Người Đô Thị dẫn lời PGS-TS. Lê Văn Truyền, Chủ tịch Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc (Bộ Y tế), cho biết Bộ Y tế đã cấp phép cho cả 3 công ty trên điều kiện cấp bách, kèm theo rất nhiều các điều kiện chi tiết trong văn bản Cục Quản lý Dược đã ban hành.
Về liều dùng, hiện liều khuyến cáo cho người trưởng thành là uống 800mg Molnupiravir mỗi 12 giờ trong 5 ngày. Độ an toàn và hiệu quả của Molnupiravir khi sử dụng trong khoảng thời gian dài hơn 5 ngày chưa được xác định. Nếu quên một liều quá 10 giờ, bệnh nhân không nên uống lại liều đã quên mà cần uống liều kế tiếp theo lịch trình. Không dùng gấp đôi liều để bù lại liều đã quên.
Giới hạn sử dụng: Không được sử dụng Molnupiravir quá 5 ngày liên tiếp. Không sử dụng Molnupiravir để dự phòng trước hay sau phơi nhiễm, không sử dụng để điều trị khởi đầu cho bệnh nhân cần nhập viện do COVID-19 do chưa ghi nhận lợi ích của Molnupiravir khi khởi đầu sử dụng ở đối tượng này. Các bệnh nhân đã được sử dụng Molnupiravir trước khi nhập viện có thể tiếp tục sử dụng thuốc cho đủ liệu trình điều trị.
Đối với phụ nữ có thai và cho con bú, Molnupiravir không được khuyến cáo sử dụng trong thời kỳ mang thai. Phụ nữ chuẩn bị mang thai nên sử dụng biện pháp tránh thai hiệu quả trong thời gian điều trị và trong 4 ngày sau liều Molnupiravir cuối cùng. Hội đồng cũng cho rằng dựa trên khả năng xảy ra các phản ứng có hại cho trẻ sơ sinh từ Molnupiravir, không khuyến cáo F0 là phụ nữ nuôi con nhỏ cho con bú trong thời gian điều trị và trong 4 ngày sau liều Molnupiravir cuối cùng.
Minh Sơn
Từ khóa thuốc điều trị COVID-19 thuốc Molnupiravir