Nhãn thuốc Molnupiravir giả ở Thụy Sĩ ‘sản xuất tại Bình Dương’ ghi sai tên địa danh
- Nguyễn Quân
- •
Trước thông tin cảnh báo về lọ thuốc Molnupiravir giả được phát hiện ở Thụy Sĩ, trên nhãn ghi “sản xuất tại Bình Dương” được công bố, Bộ Y tế và Sở Y tế tỉnh Bình Dương chưa công bố thông tin xác minh, cho hay vẫn đang tiến hành kiểm tra địa chỉ sản xuất ghi trên nhãn.
- Pháp hủy đơn đặt hàng thuốc trị COVID-19 Molnupiravir
- Tình hình COVID-19: Mỹ phê duyệt thuốc viên Molnupiravir dùng tại nhà
Ngày 6/5, tại buổi họp báo do UBND tỉnh Bình Dương tổ chức, ông Huỳnh Minh Chín, Phó Giám đốc Sở Y tế Bình Dương cho biết sau khi có thông tin thuốc giả Molnupiravir sản xuất tại Bình Dương được phát hiện tại Thụy Sỹ, cơ quan chức năng của Bộ và Sở Y tế Bình Dương đang tiến hành kiểm tra.
Theo ông Chín, đoàn kiểm tra sẽ rà soát theo địa chỉ ghi trên bao bì của lọ thuốc giả tại phường An Phú, TP Thuận An, dự kiến cuối giờ chiều nay (tức ngày 6/5) sẽ có kết quả rà soát, kiểm tra.
Tối 5/5, Cục Quản lý Dược (Bộ Y tế) có công văn gửi Sở Y tế các tỉnh, thành phố trực thuộc Trung ương về việc thuốc giả Molnupiravir phát hiện tại Thụy Sỹ, trên nhãn có thông tin tiếng Việt.
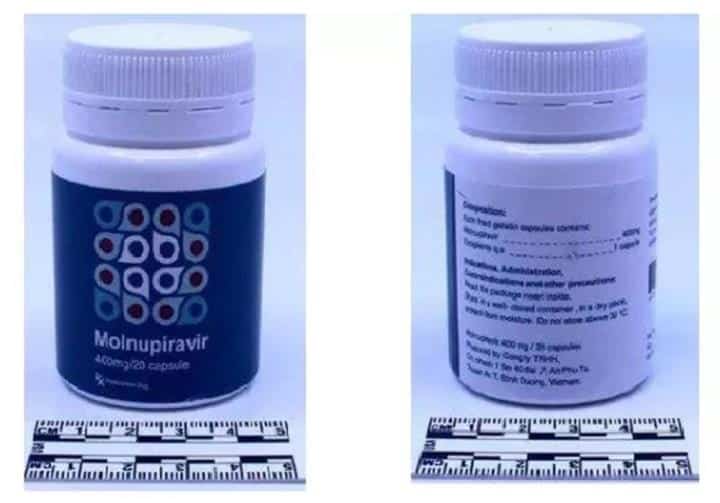
Cục Quản lý Dược cho biết nhận thông tin từ Văn phòng đại diện Tổ chức Y tế Thế giới (WHO) tại Việt Nam gửi cảnh báo khẩn từ Tổng hành dinh WHO, cho hay Hải quan Thụy Sỹ đã phát hiện thuốc giả Molnupiravir thông tin như sau: “Thuốc giả Molnupiravir 400mg, dạng bào chế nang cứng, quy cách đóng gói: Lọ 20 viên nang cứng, trên nhãn có thông tin ghi “Manufactured by Công ty TNHH, Chi nhanh 1 so 40 dai, P. An Phu, Tx. Thuan An, Tinh Binh Duong, Vietnam.”
Kết quả kiểm nghiệm thuốc cho thấy thuốc không chứa hoạt chất như ghi trên nhãn, xác định là thuốc giả.
Trên nhãn của lọ thuốc, phần xuất xứ không ghi tên công ty, địa chỉ bị thiếu, Thuận An được viết là “thị xã” dù từ đầu năm 2020, đơn vị hành chính này đã lên cấp thành phố.
Cục Quản lý Dược hiện đề nghị Sở y tế các tỉnh, thành phố thông báo cho các cơ sở kinh doanh, sử dụng thuốc và và người dân về thuốc giả Molnupiravir 400mg có các dấu hiệu nêu trên để không buôn bán, sử dụng.
Bộ Y tế yêu cầu tổ chức tiếp nhận thông tin, báo cáo của các cơ sở kinh doanh, sử dụng thuốc; phối hợp với các cơ quan chức năng liên quan kiểm tra xác minh, truy tìm nguồn gốc xuất xứ của thuốc giả nêu trên, xử lý các tổ chức, cá nhân vi phạm theo quy định hiện hành.
Molnupiravir là một trong những loại thuốc kháng virus được Bộ Y tế đưa vào phác đồ điều trị COVID-19 ở Việt Nam từ tháng 10/2021 theo đề cương thuyết minh thử nghiệm lâm sàng. Loại thuốc này đã được đưa vào sử dụng có kiểm soát trong điều trị COVID-19 tại TP.HCM từ tháng 8/2021.
Tháng 2/2022, Cục Quản lý Dược đã cấp số đăng ký lưu hành cho 3 thuốc chứa hoạt chất Molnupiravir sản xuất trong nước là: Molravir 400 của Công ty CP Dược phẩm Boston Việt Nam, Movinavir của Công ty CP hóa-dược phẩm Mekorpha và Molnupiravir Stella 400mg của Công ty TNHH Liên doanh Stellapharm.
Có nhiều nhóm người không được sử dụng hoặc khuyến cáo sử dụng thận trọng thuốc Monulpiravia trong điều trị COVID-19. Các thành viên Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc (Bộ Y tế) đã thống nhất về cảnh báo và thận trọng khi dùng thuốc Monulpiravia.
Thuốc Molnupiravir được xác định có khả năng xảy ra các phản ứng có hại đối với phụ nữ có thai và đang cho con bú, phụ nữ dự tính mang thai, trẻ sơ sinh, trẻ em và thanh thiếu niên dưới 18 tuổi, nam giới có khả năng kết hợp với người nữ có khả năng sinh đẻ. Việc sử dụng thuốc Molnupiravir cần phải có sự thăm khám, kê đơn và hướng dẫn của bác sỹ, nhân viên y tế.
Từ khóa Bình Dương thuốc giả điều trị COVID-19 thuốc Molnupiravir